ભારતની કોવેક્સીનને આ દેશમાં ઈમરજન્સી વપરાશ માટે પરવાનગી ન મળી, આ છે કારણ
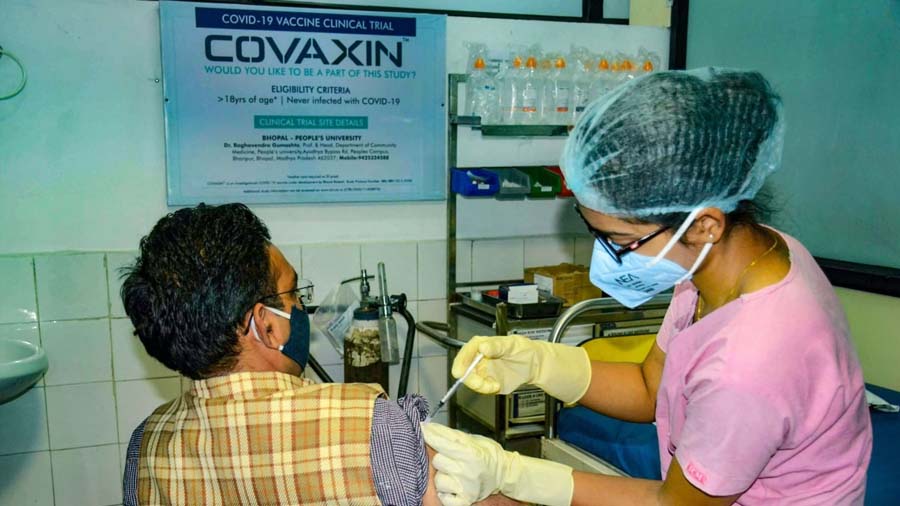
કોરોના સામેની જંગમાં કોવેક્સીન બનાવનારી સ્વદેશી કંપની ભારત બાયોટેક માટે સારા સમાચાર નથી. કોવેક્સીનને લઇ આ સમાચાર ત્યારે આવ્યા છે જ્યારે ભારત બાયોટેકે ભારતના વેક્સીનેશન કાર્યક્રમમાં કંપનીની વેક્સીનને સામેલ કરવાના લગભગ 6 મહિના પછી પોતાના ત્રીજા સ્ટેજના ક્લિનિકલ પરીક્ષણના ડેટા શેર નહીં કરવા માટે ભારતમાં ટીકાઓનો સામનો કરવો પડી રહ્યો છે.
ભારત બાયોટેકે પોતાની કોરોના વેક્સીન કોવેક્સીનના ફેઝ 3ના ડેટાને વૈજ્ઞાનિક પત્રિકાઓને આપ્યા પછીના બે-ચાર મહિનામાં વેક્સીનના વિશેષજ્ઞો દ્વારા પીયર રિવ્યૂ(સમીક્ષા)ની આશા છે. કંપનીએ હજુ સુધી આ વેક્સીનના ડેટા સાર્વજનિક કર્યા નથી. કોવેક્સીનની ત્રીજા સ્ટેજની ટ્રાયલમાં લગભગ 25800 લોકોએ ભાગ લીધો હતો.
ખેર, તો બીજી તરફ અમેરિકામાં ભારત બાયોટેકની કોવેક્સીનના ઈમરજન્સી વપરાશને મંજૂરી મળી નથી. અમેરિકાના FDAએ ભારત બાયોટેકની કોરોના વેક્સીનના ઈમરજન્સી વપરાશની અરજીને ફગાવી દીધી છે. જેના કારણે અમેરિકામાં કંપનીની વેક્સીન લોન્ચ થવામાં વાર લાગશે. પાછલા દિવસોમાં ભારત બાયોટેકની કોવેક્સીન માટે અમેરિકાના ભાગીદાર ઓક્યૂઝેને FDAની પાસે માસ્ટર ફાઇલ મોકલીને આ વેક્સીનના ઇમરજન્સી વપરાશ માટે મંજૂરી માગી હતી.
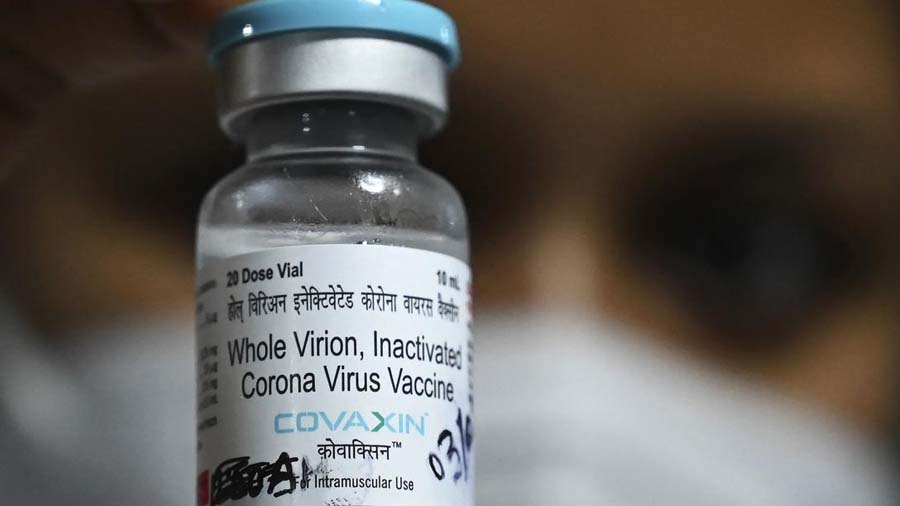
ઓક્યૂઝેને ગુરુવારે કહ્યું કે, કંપની હવે કોવેક્સીનની સંપૂર્ણ મંજૂરી માગશે. અમેરિકામાં FDA કંપનીને એક અતિરિક્ત પરિક્ષણ શરૂ કરવા કહી રહ્યું છે જેથી કંપની એક બાયોલોજિક્સ લાયસન્સ માટે અરજી માટે ફાઇલ કરી શકે. જે એક પૂર્ણ મંજૂરી છે. FDAએ ભલામણ કરી હતી કે ઓક્યૂઝેન પોતાની વેક્સીન માટે ઈમરજન્સી યૂઝ ઓથોરાઇઝેશનની અરજી કરવાના સ્થાને BLA (બાયોલોજિક્સ લાયસન્સ અરજી) સબમિશન પર ફોકસ કરે. સાથે જ FDAએ વેક્સીનના સંબંધમાં વધારે જાણકારી અને ડેટાનો આગ્રહ કર્યો છે.
ઓક્યૂઝેને કહ્યું કે, કંપની પોતાની વેક્સીનની અરજીને મંજૂરી મળે તેના માટે જરૂરી વધારાના દસ્તાવેજોને લઇ FDA સાથે ચર્ચા કરી રહી છે. ઓક્યૂઝેનના મુખ્ય કાર્યકારી શંકર મુસુનીરીએ કહ્યું કે ભલે આના કારણે વેક્સીન અમેરિકામાં આવવામાં વાર લાગે પણ અમે કોવેક્સીન માટે કટિબદ્ધ છીએ. જણાવી દઇએ કે, ઓક્યૂઝેને FDAની પાસે સમીક્ષા માટે પ્રીક્લિનિકલ સ્ટડી, રસાયણ, વિનિર્માણ અને નિયંત્રણ(સીએમસી) અને ક્લિનિકલ અધ્યયનના પરીણામોને માસ્ટર ફાઇલના રૂપમાં મોકલ્યા હતા.

કંપનીએ પોતાના એક નિવેદનમાં કહ્યું કે, FDAની આ પ્રતિક્રિયા(મંજૂરી ન આપવાની) ઓક્યૂઝેનની એ માસ્ટર ફાઇલને લઇ હતી, જેને કંપનીએ પાછલા દિવસોમાં FDAને જમા કરાવી હતી. FDAએ ભલામણ કરી હતી કે ઓક્યૂઝેન પોતાની વેક્સીન માટે ઈમરજન્સી યૂઝ ઓથોરાઇઝેશનની(EUA) અરજી કરવાના સ્થાને BLA (બાયોલોજિક્સ લાયસન્સ અરજી) સબમિશન પર ફોકસ કરે.
નીચે આપેલી લીંક પર ક્લિક કરીને જોડાઓ khabarchhe.com ન્યૂઝ સાથે.
તમે અમને ફેસબુક, ટ્વીટર, ટેલીગ્રામ, ઇન્સ્ટાગ્રામ અને યુ ટ્યુબ પર પણ લાઇક અને ફોલો કરી શકો છો.
લેટેસ્ટ ન્યૂઝ અપડેટ્સ તમારા ફોન પર સૌથી પહેલા મેળવવા માટે આજે જ ડાઉનલોડ કરો khabarchhe.com ની મોબાઇલ એપ્લિકેશન.
ગુજરાતનું અગ્રેસર ન્યૂઝ પોર્ટલ, અહીં વાત થાય છે માત્ર ગુજરાત અને ગુજરાતનાં હિતની... Download Khabarchhe APP www.khabarchhe.com/downloadApp

